2013年に東京都健康安全研究センター並びに都・区検査機関、都内の病院、登録衛生検査所等で分離された赤痢菌とサルモネラを対象に、菌種、血清型別および薬剤感受性試験の成績についてまとめたので、その概略を紹介する。チフス菌およびパラチフスA菌については、国立感染症研究所(感染研)に依頼したファージ型別の成績も併せて紹介する。
供試菌株は、都内の患者とその関係者および保菌者検索事業によって分離された赤痢菌29株(海外旅行者由来:21、国内事例由来:8)、サルモネラ134株(海外:1、国内:133)、チフス菌21株(海外:10、国内:11)およびパラチフスA菌11株(全て海外旅行者由来)である。
血清型別は、常法により行った。薬剤感受性試験は、米国臨床検査標準化協会(CLSI:Clinical and Laboratory Standards Institute, 旧NCCLS)の抗菌薬ディスク感受性試験実施基準に基づき、市販の感受性試験用ディスク(センシディスク:BD)を用いて行った。供試薬剤は、クロラムフェニコール(CP)、テトラサイクリン(TC)、ストレプトマイシン(SM)、カナマイシン(KM)、アンピシリン(ABPC)、スルファメトキサゾール・トリメトプリム合剤(ST)、ナリジクス酸(NA)、ホスホマイシン(FOM)、ノルフロキサシン(NFLX)およびセフォタキシム(CTX)の10剤である。NA耐性株についてはEtest(シスメックス・ビオメリュー)を用いてシプロフロキサシン(CPFX)、レボフロキサシン(LVFX)、オフロキサシン(OFLX)、NFLXの4種類のフルオロキノロン系薬剤に対する最小発育阻止濃度(MIC:μg/ml)を測定した。
また、CTX耐性の菌株については、Extended-spectrum β-lactamase (ESBL)産生菌であることを疑い、セフポドキシム(CPDX)、セフタジジム(CAZ)、セフトリアキソン(CTRX)、アズトレオナム(AZT)、セフォタキシム(CTX)およびアモキシシリン・クラブラン酸合剤(AMPC/CVA)の感受性試験用ディスク(BD)を用いたDouble disk synergy testおよびEtestにより、クラブラン酸によるβ-ラクタマーゼ活性阻害の有無を確認した。
1.赤痢菌
赤痢菌の菌種および耐性菌の出現頻度を表1に示した。
赤痢菌29株の菌種別内訳は、フレキシネル菌11株(海外:6、国内:5)、ソンネ菌18株(海外:15、国内:3)であり、ディセンテリ―菌およびボイド菌は検出されなかった。全ての株がいずれかの薬剤に耐性を示し(耐性率100%)、その薬剤別耐性頻度は、SM(86.2%)、TC(79.3%)、ST(58.6%)、NA(55.2%)、ABPC(51.7%)、NFLX(27.6%)、CP(24.1%)、CTX(3.4%)の順であった。なお、KM、FOMに耐性を示す株は認められなかった。
NA耐性を示した13株(全て海外由来)について、フルオロキノロン系薬剤に対するMICを測定した結果、7株は耐性(CPFX:4~8μg/ml、LVFX:4~8μg/ml、OFLX:8~32μg/ml、NFLX:16~32μg/ml)、1株は中間(CPFX:4μg/ml、LVFX:4μg/ml、OFLX:8μg/ml、NFLX:16μg/ml)を示し、残る5株は低感受性(MIC:0.1~1.0μg/ml)であった。耐性7株はフレキシネル2a(2株)およびソンネ(5株)であった。このフレキシネル菌2株はインドおよびネパールからの帰国者から検出されたものであり、ソンネ菌5株は全てインド由来株であった。
CTX耐性株はソンネ菌1株に認められ、国内事例由来株であった。薬剤耐性パターンは「SM・ABPC・NA・CTX」で、CTX-M-1型遺伝子を保有するESBL産生菌であることが確認された。
2.チフス菌およびパラチフスA菌
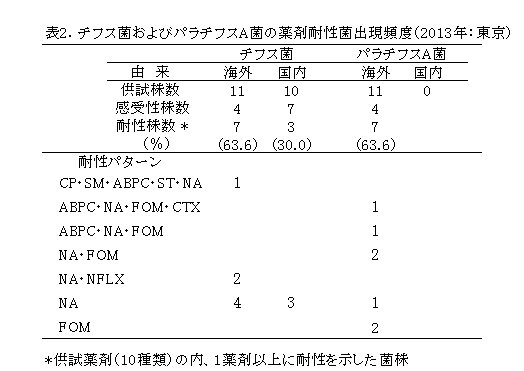
薬剤耐性菌出現頻度および薬剤耐性パターンを表2に示した。チフス菌21株は海外由来11株、国内由来10株であった。海外由来株のうち7株(63.6%)は供試した薬剤のうちいずれかに耐性を示し、NA単剤耐性が4株、「NA・NFLX」の2剤耐性が2株、「CP・SM・ABPC・ST・NA」の5剤耐性が1株であった。国内由来株10株中、いずれかの薬剤に耐性を示したものは3株(30.0%)で、全てNA単剤耐性株であった。
パラチフスA菌11株(全て海外)中7株(63.6%)が耐性株で、「NA・FOM」の2剤耐性が2株、FOM単剤耐性が2株、その他「ABPC・NA・FOM・CTX」、「ABPC・NA・FOM」およびNA単剤耐性株がそれぞれ1株であった。チフス菌21株についてのファージ型別結果は、A型(4株)、B1型(2株)、E1型(6株)、E2型(2株)、E9型(1株)、M1型1株、UVS(Untypable Vi strain)1型(3株)、UVS4型(2株)であった。パラチフスA菌11株のファージ型は、1型(4株)、2型(3株)、4型(1株)、UT(Untypable)型(3株)であった。
注目すべき点として、2013年は国内事例由来の腸チフスの発生が多かったことがあげられる。2008年から2012年の国内事例由来のチフス菌分離は年間0~2株であったが、2013年には11株と急増した。特に半数以上にあたる6株が10月以降に分離されており、その薬剤耐性パターンはNA単剤耐性が1株、感受性株が5株であった。感受性株5株のファージ型はA型(3株)、(B1型)2株であった。感染研で実施したMultiple-Locus Variable-Number Tandem-Repeats Analysis(MLVA)ではこれら5株は同一のクラスターを形成しており、何らかの共通感染源の存在の可能性も考えられたが、詳細は不明であった(感染研:病原微生物検出情報 35: 115-116, 2014 http://www.nih.go.jp/niid/ja/id/1011-disease-based/ta/typhi/idsc/iasr-in/4702-kj4101.html )。
3.チフス菌およびパラチフスA菌以外のサルモネラ
チフス菌・パラチフスA菌以外のサルモネラ134株(海外:1、国内:133)の血清型および耐性菌の出現頻度を表3に示した。O群別内訳は、O4群46株(34.3%)、O7群35株(26.1%)、O8群35株(26.1%)、O9群8株(6.0%)、O3,10群5株(3.7%)、O1,3,19群2株(1.5%)、O6,14群、O13群、O28群、O38群が各1株(0.7%)であった。O4群、O7群、O8群およびO9群で全体の92.5%を占めた。主な血清型は、S. Typhimurium(O4群,12株)、S. Thompson(O7群,12株) 、O4 : i : – (10株)、S. Manhattan(O8群,8株)、S. Newport(O8群,8株)であった。
サルモネラ134株中46株(34.3%)が耐性株で、前年(20.0%)と比べて耐性頻度はやや増加した。各薬剤に対する耐性頻度は、TC(30.6%)、SM(21.6%)、ABPC(15.7%)、NA(8.2%)、KM(7.5%)、CP (3.7%)、ST (3.7%)、 NFLX(1.5%)、CTX(1.5%)であった。なお、FOM耐性株は認められなかった。薬剤耐性パターンは20種で、「TC・SM」(10株)、「TC・SM・ABPC」(8株)が主要なものであった。O群別の耐性頻度では、O4群(54.4%)、O9群(50.0%)およびO8群(31.4%)が高かった。最も多く検出された血清型であるS. Typhimuriumの耐性頻度は58.3%で、ABPC(50.0%)、TC(41.7%)、SM(41.7%)に耐性の株が多くみられた。
フルオロキノロン系薬剤であるNFLXに耐性を示した1株の血清型は、S. Kentucky(O8群)であり、薬剤耐性パターンは「TC・ABPC・NA・NFLX」の4剤耐性菌であった。CTXに耐性を示した2株は、S. AgonaおよびO4 : i :‐で、両株共にTEMおよびCTX-M-1型遺伝子を保有するESBL産生菌であることが確認された。
今後もこれら耐性菌は増加する事が予想される。また、国内事例由来の赤痢菌やチフス菌については、広域散発例の可能性が否定できない事例も発生しており、菌株の疫学解析は益々重要となる。引き続き、その動向を注意深く監視する必要がある。
(微生物部 食品微生物研究科 腸内細菌研究室)